—— PROUCTS LIST
如何補償溫度對pH電極測試的影響?
溶液pH值跟溫度的關系
pH即溶液的酸堿度,嚴格上說就是氫離子活度的負對數,在25度下中性溶液pH值為7.0,小于7的為酸性溶液,大于7的為堿性溶液。不同溫度下測試出來的pH值是不一樣的,你們知道是為什么嗎?
原因如下:
- 電極斜率
我們都是用pH電極來測試溶液的pH值的,電極的電化學基本工作原理是基于能斯特方程,在這個方程式中,有個K(電極斜率),電極斜率K=2.303 RT/nF,與溫度有關。一般溫度系數f=3.35×10-3/℃ 。在25度下,理論值K=-59.16 mV/pH。
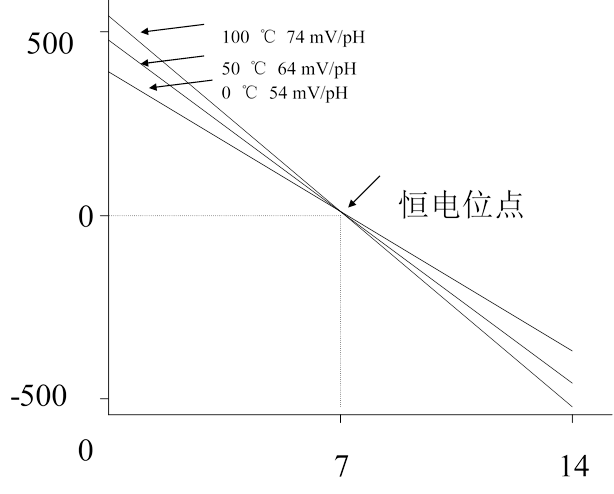
補償方式:接一個溫度探頭自動補償,或手動輸入當前溫度手動補償
美國BJC的S400-RT33D-E10FF在線pH電極就內置了Pt100的溫度探頭。
- pH緩沖液
l 溶液的化學平衡性與溫度有關。
l 由于緩沖液化學成分已知,pH與溫度有恒定關系。
l 為使測試準確,在校正時要輸入當前溫度下的標準液pH值!!
比如NIST緩沖液(6.86)在不同的溫度條件下有不同的pH值:6.86(25C), 6.87(20C), 6.85(30C), 6.92(10C)。
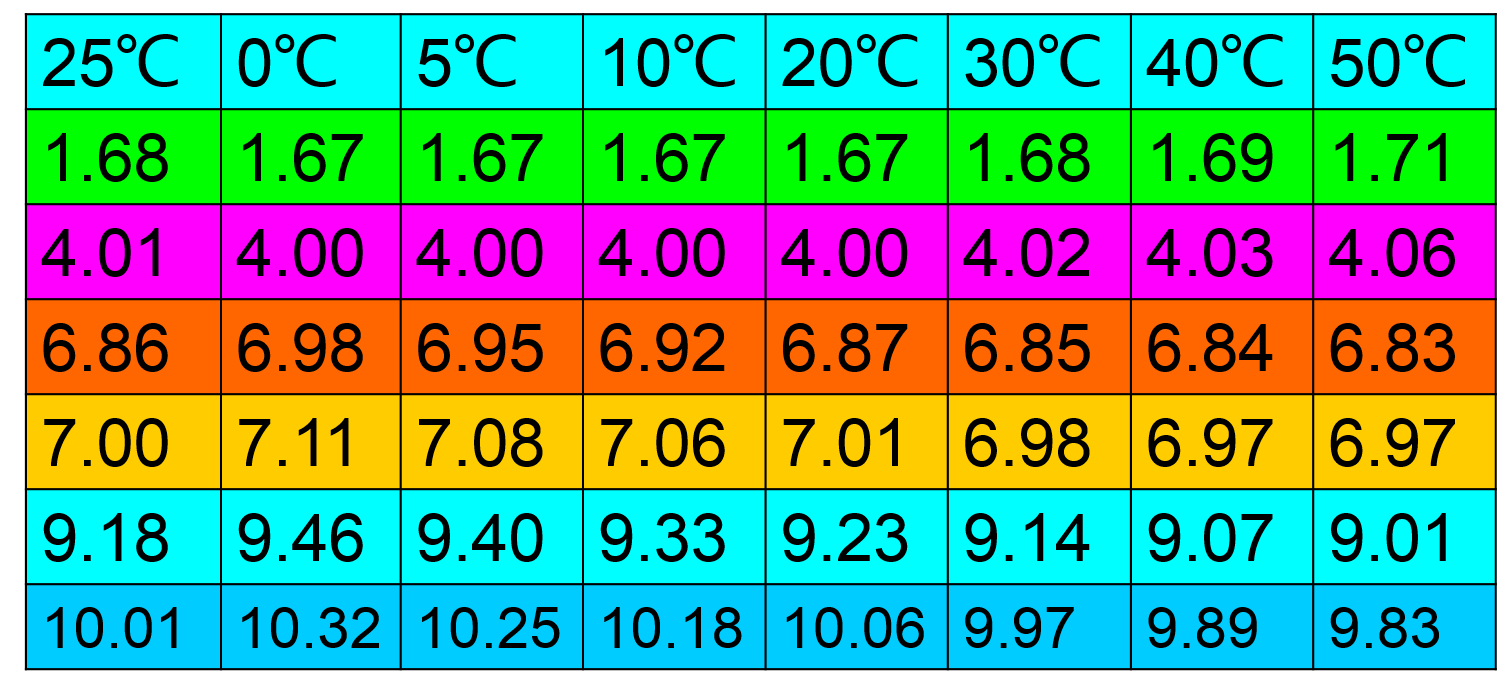
- 樣品pH值與溫度
l 由于樣品化學成分各不相同,它們的pH值與溫度變化關系不可預知,因此必須在同一溫度下測試和校正,在報告pH值時要注明測試溫度。
l 使用ATC探頭,使測試更準確。
- 參比元件漂移
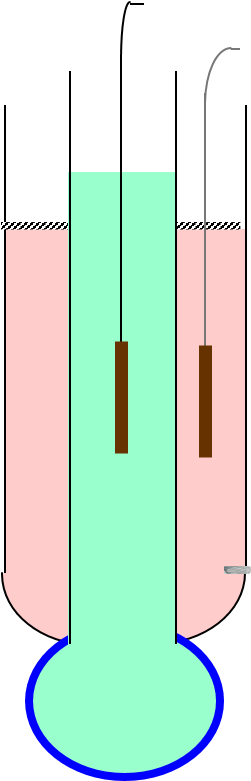
l 當溫度變化時,pH感測電極與參比電極的內部參比元件要有一個達到熱平衡的過程,在這過程中會使pH測值漂移,不穩定。
l 該過程越短越好。
l 影響電極反應速度。
l 溫度電極誤差
- 測試溫度變化顯著的溶液時,讀數會不穩、漂移,原因如下:
l 溫度探頭與pH電極的溫度特性不一致,影響熱平衡。
l 溶液內部各點溫度并不*一致。
如何減少溫度影響?
l 使用三合一電極,使pH電極感測點與溫度感測點盡可能接近。
l 有些技術,通過感測pH玻璃敏感膜的電阻變化來感測溶液溫度。
l 或者在pH電極頭上有個溫度晶片。
后兩種價格較貴,且要與特殊的主機配套使用。

